¿cual es la diferencia entre iónico y covalente?
La mayoría de los compuestos utilizados en química pueden ser iónicos o covalentes. Estos tipos de compuestos tienden a diferir en términos de enlace y transferencia de electricidad.
La principal diferencia entre los compuestos iónicos y covalentes en forma tabular es que los compuestos iónicos son metales con enlaces iónicos, mientras que los compuestos covalentes son no metales con enlaces covalentes.
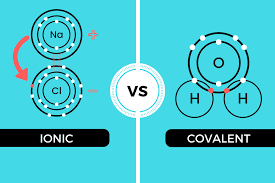
¿Qué son los compuestos iónicos?
Los compuestos iónicos se refieren a compuestos metálicos que tienen cargas eléctricas opuestas. Esto implica que la fuerza electrostática entre cada átomo tiende a atraerse entre sí.
El compuesto puede perder o ganar un electrón adicional en la capa más externa para lograr una configuración electrónica estable.
Los cationes son compuestos iónicos que ceden un electrón extra de la capa exterior para tener un estado estable y cargarse positivamente.
Por otro lado, los aniones son compuestos iónicos que ganan un electrón extra en la capa externa para tener una configuración estable y cargarse negativamente.
Por lo tanto, los enlaces iónicos en los compuestos iónicos se producen como resultado de aniones y cationes. Sigue leyendo para notar la diferencia entre sólido iónico y sólido covalente.
¿Qué son los compuestos covalentes?
Los compuestos covalentes son compuestos no metálicos que resultan en la formación de un enlace covalente débil. Estos compuestos normalmente se encuentran en estado gaseoso.
El sólido covalente alcanza una configuración electrónica estable al compartir electrones en un espacio orbital superpuesto común.
Los átomos del sólido covalente se juntan en una superposición orbital antes de compartir los electrones en su capa más externa.
El compuesto resultante tiende a ser neutro ya que ninguno de los átomos está cargado. La superposición tiende a ocurrir en un patrón lineal.
Cuadro comparativo: compuestos iónicos y covalentes
Términos básicos Compuestos iónicos Compuestos covalentes Significado Estos son compuestos con enlace iónico donde los átomos se atraen electrostáticamente entre sí Estos son compuestos donde los electrones se comparten entre los átomos involucrados en la formación Especies involucradas Interacción de aniones y cationes Interacción de átomos neutros Tipo de enlace Enlaces iónicos Covalente enlaces Fuerza del enlace Fuerte Débil Metálico o no metálico Metálico No metálico Conductividad eléctrica Buen conductor en forma líquida o media No es un buen conductor Estado de la materia Medio al estado líquido Estado gaseoso Ionización Tiende a ionizarse en una solución fundida No ionizar en absoluto Solubilidad en solvente orgánico No se disuelve Tiende a disolverse Forma o apariencia Tiene una forma definida No tiene una forma definida
Diferencia principal entre compuestos iónicos y covalentes
Leer más: Diferencia entre entropía y entalpía
Vídeo comparativo
Resumen
Por lo tanto, los compuestos iónicos son buenos conductores de electricidad debido a la interacción de cationes y aniones. Por otro lado, los compuestos covalentes no conducen la electricidad debido a la interacción de los átomos neutros. Esta es la diferencia central entre el compuesto iónico y el compuesto covalente cerebralmente.